顶空-气相色谱仪法同时检测一次性使用无菌医疗器械产品中环氧乙烷和2-氯乙醇残留量
灭菌是确保医疗器械安全性和有效性的有效途径。环氧乙烷(ethylene oxide,EO)具有广谱高效杀菌作用,且成本较低、穿透性强,属目前常用的高效化学低温灭菌剂之一[1],在一次性使用无菌医疗器械灭菌中被广泛应用[2-3]。但EO具有致突变性、胎儿毒性和致畸特性,且对睾丸功能具有不良作用,并能对人体多个器官系统产生损害[4-6]。且在医疗器械的生产、灭菌、存储、运输、使用等环节中,EO残留物会生成其他副产物。有研究发现,残留的EO可发生水解,进而与产品或环境中的氯离子反应生成2-氯乙醇(ethylene chlorohydrin,ECH)[1]。而ECH同样具有致突变性、胎儿毒性和致畸特性,并可损害人体的肺、肾、中枢神经系统和心血管系统[4]。因此,对采用EO灭菌的一次性使用无菌医疗器械产品中EO和ECH的残留量进行检测具有重要意义。
现有研究多采用顶空-气相色谱法和气相色谱-质谱联用法进行EO和ECH残留量的同时检测,且多集中于食品和药品领域的检测[7-10]。目前关于可同时检测一次性使用无菌医疗器械产品中EO和ECH残留量方法的报道相对较少。林红赛等[11]以一次性使用动脉止血压迫器为例,探讨顶空-气相色谱法同时检测EO灭菌残留EO和ECH的效果,但未对检测方法的顶空条件进行探讨。尹戈等[12]采用顶空-气相色谱法检测医用口罩和防护服中EO和ECH的残留量,但该研究直接设定平衡温度为90℃,未探讨其他温度对检测结果的影响。基于此,本研究采用水为浸提介质,通过优化平衡温度、平衡时间,得到最佳顶空条件,并选取了最佳浸提比例,在此基础上分析顶空-气相色谱法的检测价值,并采用该方法分析EO灭菌的典型一次性使用无菌医疗器械产品中EO和ECH的残留量,以期为相关产品的监督检测提供参考。
1 实验仪器与方法
1.1 仪器与试剂
顶空-气相色谱仪,配有氢火焰离子化检测器和自动顶空进样器;超纯水机;电子天平;移液器(型号:100~1 000μl、0.5~5 ml、1~10 ml)。
EO(河南标准物质研发中心,规格:10 mg/ml,5 ml/支);ECH(PANPHY Chemicals Corporation,规格:100 mg/支)。
本实验所用一次性使用无菌医疗器械产品均为我单位购买的科研用产品,且均经EO灭菌,包括一次性使用聚氯乙烯输液器、一次性使用TPE输液器、一次性使用聚氯乙烯鼻氧管、一次性使用医用口罩、医用棉垫共5种产品,厂家信息不予公开。
1.2 标准品溶液的配制
1.2.1 EO和ECH混合贮备液的配制
精密量取1.00 ml EO并精密称重100.00 mg ECH分别置于100 ml容量瓶(已加约80 ml纯水)中,用水定容得到浓度分别为100.00μg/ml EO和1 000.00μg/ml ECH的混合贮备液。
1.2.2 标准品溶液的配制
分别精密量取EO和ECH混合贮备液0.125、0.25、0.50、1.00、2.50、5.00、7.50、10.00 ml置于50 ml容量瓶(已加约40 ml纯水)中,加水定容得到EO浓度依次为0.25、0.50、1.00、2.00、5.00、10.00、15.00、20.00μg/ml和ECH浓度依次为2.50、5.00、10.00、20.00、50.00、100.00、150.00、200.00μg/ml的标准品溶液。分别精密量取5.00 ml EO和ECH标准品溶液置于20 ml顶空瓶中,压盖、摇匀后置于自动顶空进样器,平行制备3份。
1.3 气相色谱仪条件的确定
1.3.1 色谱柱的选择
可用于EO和ECH检测的色谱柱包括强极性毛细管柱HP-INNOWAX[13]和DB-WAX[14]、中等极性毛细管柱DB-624[8,10-11]。以上3种毛细管柱均可对EO和ECH的分离度、响应和峰形等进行评估。而DB-624毛细管柱能在10 min内分离EO和ECH,且两者的峰形尖锐、响应值高、分离效果最好。因此,本研究选择DB-624毛细管柱对一次性使用无菌医疗器械产品进行EO和ECH残留量的检测,毛细管柱内径为1.8μm、长度为30 m、壁厚为0.32 mm。
1.3.2 其他气相色谱仪条件
柱温升温程序:50℃保持5 min,30℃/min升温至100℃保持3.333 min。进样口温度:200℃。检测器温度:250℃。载气:氮气,流速1.5 ml/min,分流比20∶1。
1.4 顶空条件的确定
1.4.1 平衡温度和平衡时间的确定
取包装完整的经验证不含EO和ECH的一次性使用聚氯乙烯输液器,称取2.50 g,剪碎,置于20 ml顶空瓶中,精密加入5.00 ml纯水,压盖,摇匀,平行制备3份。向3份样品中分别加入5.00 ml的5.00μg/ml EO和50.00μg/ml ECH、10.00μg/ml EO和100.00μg/ml ECH、20.00μg/ml EO和200.00μg/ml ECH的标准品溶液,即EO加入量分别为25.00、50.00、100.00μg,ECH加入量分别为250.00、500.00、1 000.00μg。然后,分别选择50、60、70、80℃的平衡温度和10、20、30、40 min的平衡时间,用顶空-气相色谱仪检测色谱峰面积。以平衡时间为横坐标,分别以EO和ECH的色谱峰面积为纵坐标绘制图1和图2。
由图1和图2可知,在平衡时间相同的条件下,EO和ECH的色谱峰面积随平衡温度的升高而增大。这是由于在一定范围内,温度越高EO和ECH越容易被气化,EO和ECH气体的浓度越高,色谱峰面积越大。此外,随着平衡时间的延长,EO的色谱峰面积首先增加,再趋于平稳状态。但当平衡温度为80℃、平衡时间为40 min时EO的色谱峰面积明显下降。这可能是由于温度过高导致EO发生降解,进而导致色谱峰面积下降。因此,EO检测的最佳平衡温度为80℃,最佳平衡时间为30 min。相较于EO,ECH的沸点较高,实验温度下ECH的色谱峰面积随着平衡时间的延长逐渐上升至平稳状态,说明高温度长时间浸提有助于增加ECH的色谱峰面积。因此,为同时实现EO和ECH较好的浸提效果,本研究综合考虑平衡温度和平衡时间对EO和ECH色谱峰面积的影响,选择平衡温度为80℃、平衡时间为30 min作为最佳顶空条件。
图1 平衡温度和平衡时间对EO色谱峰面积的影响
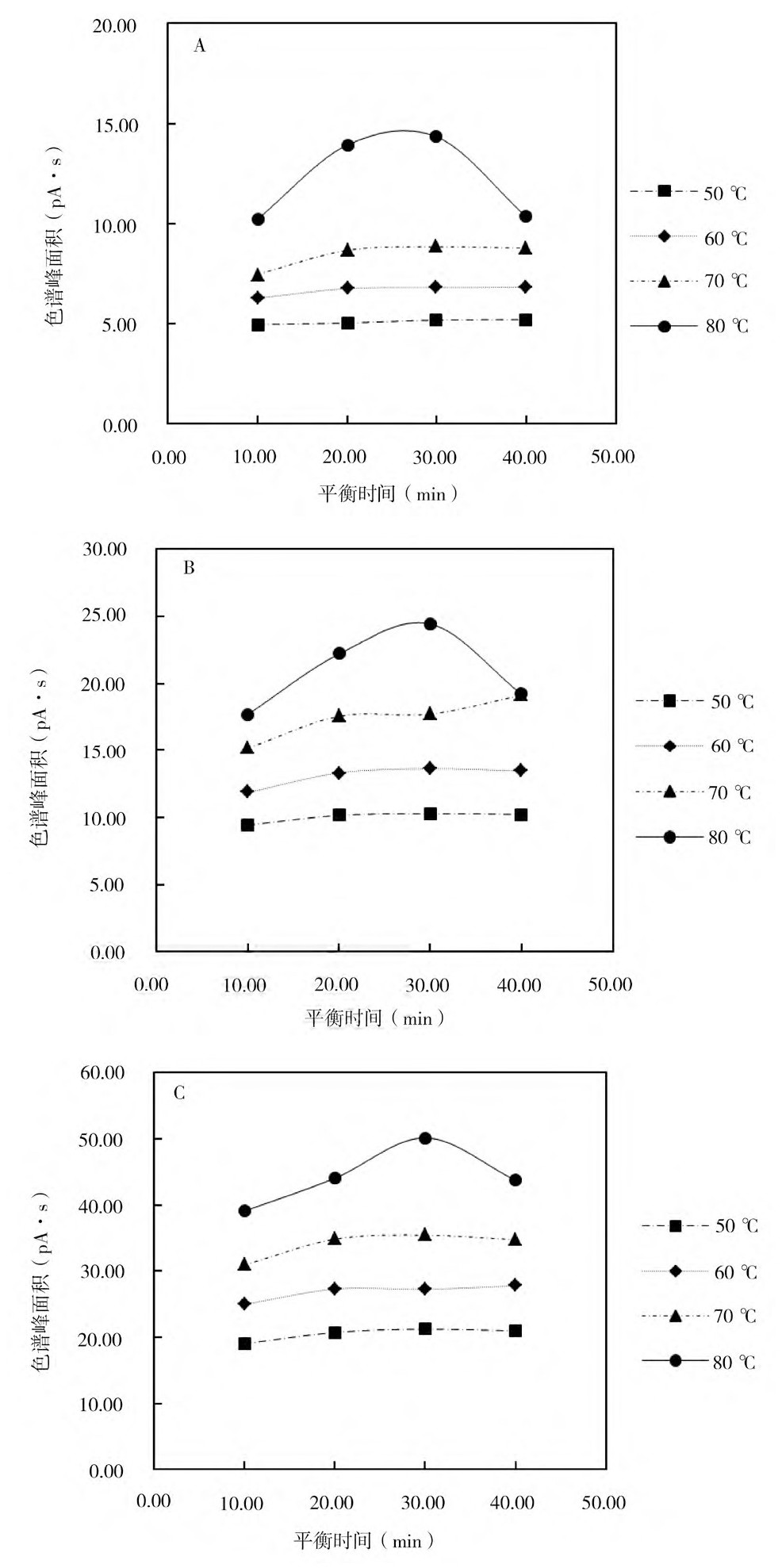
注:A、B、C对应的EO加入量分别为25.00、50.00、100.00μg;EO为环氧乙烷
1.4.2 其他顶空条件
定量环温度:90℃。传输线温度:110℃。气相色谱(gas chromatographic,GC)循环时间:12 min。
图2 平衡温度和平衡时间对ECH色谱峰面积的影响
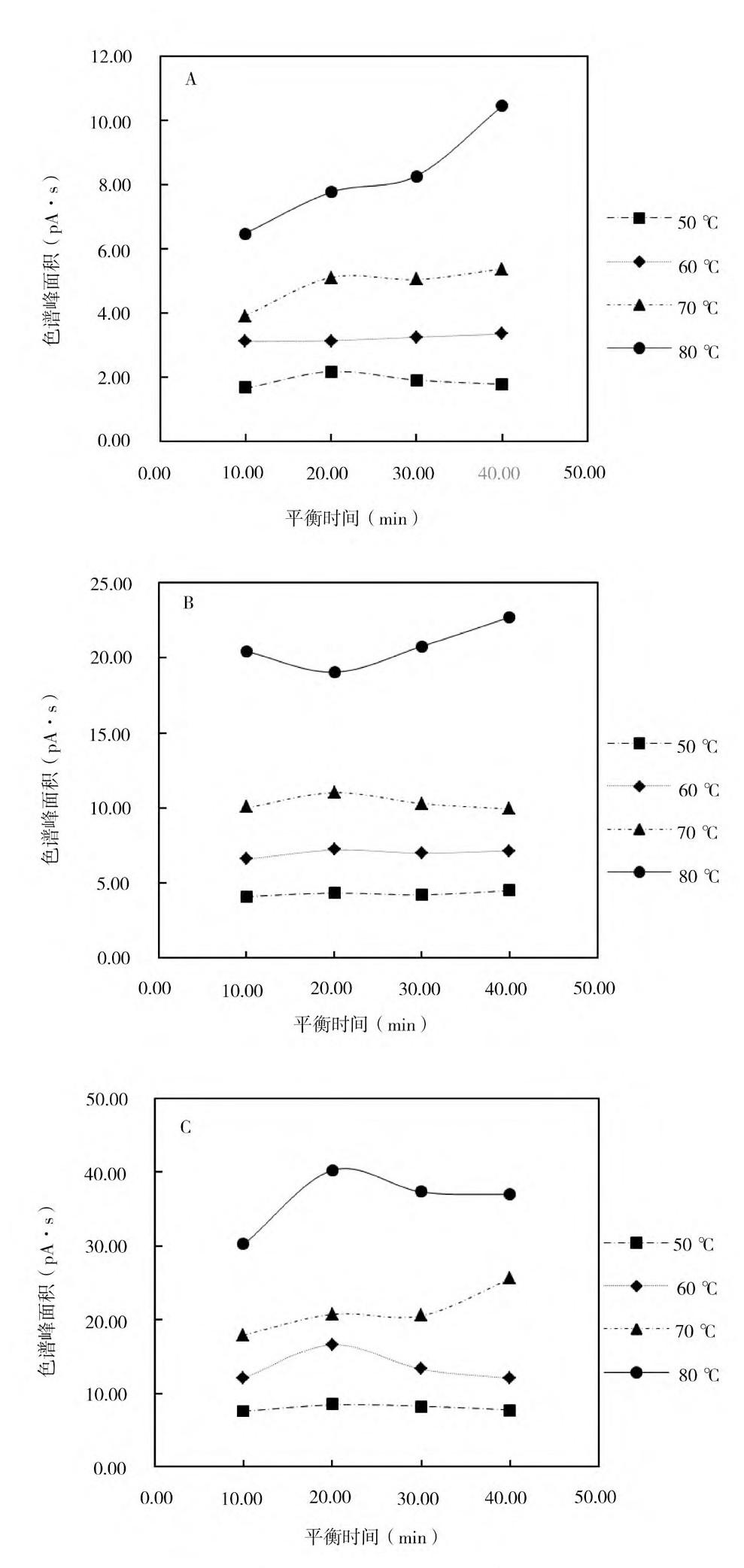
注:A、B、C对应的ECH加入量分别为250.00、500.00、1 000.00μg;ECH为2-氯乙醇
1.5 样品浸提液的配制
1.5.1 浸提比例的确定
分别取0.50、1.00、1.50、2.00、2.50、3.00、4.00、5.00 g经验证含EO和ECH残留物的一次性使用聚氯乙烯输液器样品置于顶空瓶中,精密加入5.00 ml纯水,密封,得到浓度分别为0.1、0.2、0.3、0.4、0.5、0.6、0.8、1.0 g/ml的样品。每个浓度的样品平行制备3份。在1.4确认的最佳顶空条件下采用顶空-气相色谱仪进行检测。结果发现,EO和ECH的色谱峰面积均随样品量的增加呈现先增大再趋于平稳然后再增大的趋势,见图3。考虑到当浸提比例高于0.5 g/ml时,样品在顶空瓶内所占体积较大,导致水无法完全浸湿样品表面,无法代表实际使用时带来的最大风险。因此,本研究选择0.5 g/ml的浸提比例制备样品浸提液,即样品取样量为2.50 g。
图3 浸提比例对EO和ECH色谱峰面积的影响
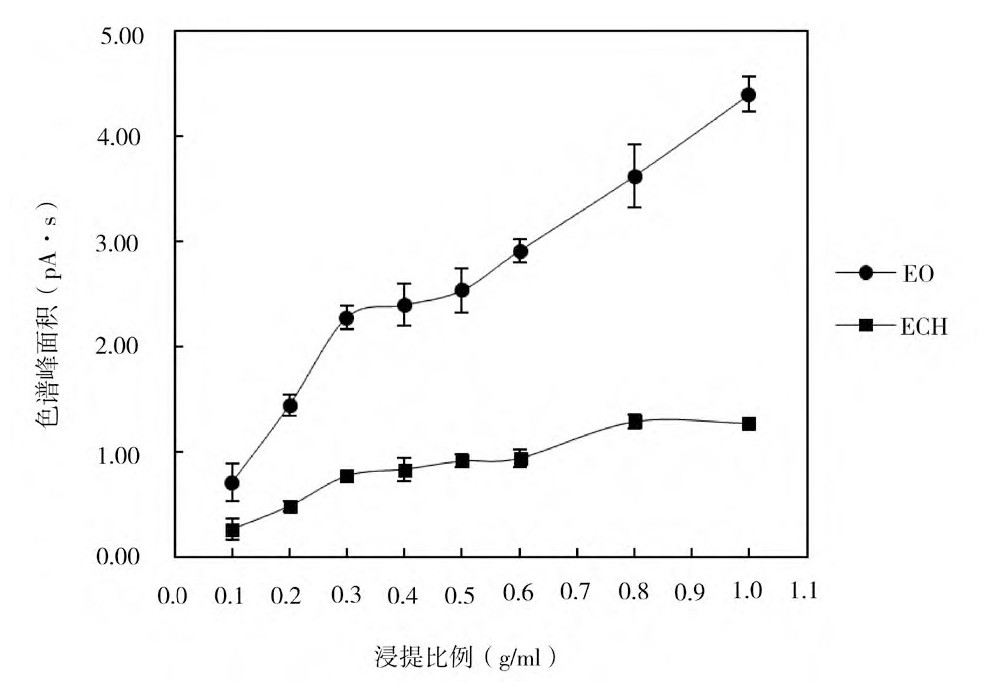
注:EO为环氧乙烷,ECH为2-氯乙醇
1.5.2 样品浸提液配制
取包装完整的一次性使用无菌医疗器械产品,称取2.50 g,剪碎,置于20 ml顶空瓶中,精密加入5.00 ml纯水,压盖,摇匀,置于自动顶空进样器。样品浸提液平行制备2份。同法制备空白溶液。
1.6 验证指标
1.6.1 专属性验证
专属性是指其他成分(如杂质、降解产物、辅料等)可能存在的情况下采用的分析方法能正确检测被测物的能力,色谱法中的分离度应符合要求(一般分离度要求>1.5)[15]。分别取空白溶液、标准品溶液的顶空瓶注入气相色谱仪,按照1.3确认的气相色谱仪条件和1.4确认的最佳顶空条件进行检测,记录色谱图。
1.6.2 线性关系与检出限、定量限验证
线性关系是指在设计的范围内,线性实验结果与试样中被测物浓度直接成正比的能力。标准曲线的线性系数最低宜为0.95[4,15]。根据1.6.1中标准品溶液的检测结果绘制标准曲线,分析EO和ECH的线性关系。
检出限是指试样中被测物质能被检测出的最低量,定量限是指试样中被测物能被定量检测的最低量[15]。通过逐级稀释标准品溶液(即将一定体积的高浓度溶液逐步稀释成低浓度溶液),按照相同条件重复进样检测,根据信号与噪声的比值确定检出限和定量限。本研究以3倍信噪比确定检出限,10倍信噪比确定定量限[16]。
1.6.3 精密度验证
精密度是指在规定的检测条件下,同1份均匀供试品经多次取样检测所得结果之间的接近程度,需计算检测结果的相对标准偏差[15]。分别将5.00 ml的1.00μg/ml EO和10.00μg/ml ECH、10.00μg/ml EO和100.00μg/ml ECH、20.00μg/ml EO和200.00μg/ml ECH混合标准品溶液置于顶空瓶中,密封,摇匀,置于自动顶空进样器后采用气相色谱仪检测。每种混合标准品溶液分别单独检测6次。
1.6.4 回收率验证
回收率是评价方法准确度的指标,即评价所建立方法的检测结果与真实值或参比值接近的程度,需计算检测结果与真实值的百分比[15]。分别取经验证不含EO和ECH的一次性使用聚氯乙烯输液器和一次性使用聚氯乙烯鼻氧管,制成浓度分别为1.00μg/ml EO和10.00μg/ml ECH、10.00μg/ml EO和100.00μg/ml ECH、20.00μg/ml EO和200.00μg/ml ECH的2种混合基质浸提液。分别取5.00 ml混合浸提液置于顶空瓶中,密封,摇匀,置于自动顶空进样器后采用气相色谱仪检测。每种混合浸提液分别单独检测6次。
1.6.5 典型产品检测
按1.5.2方法制备5个品种的一次性使用无菌医疗器械产品(一次性使用聚氯乙烯输液器、一次性使用TPE输液器、一次性使用聚氯乙烯鼻氧管、一次性使用医用口罩、医用棉垫)的样品浸提液,按照最佳的气相色谱仪条件和顶空条件进行检测,以色谱峰面积外标法(检测得到样品目标物质的色谱峰面积,根据标准曲线方程计算目标物质的浓度)计算样品中EO和ECH的残留量。
2 结果
2.1 专属性验证结果
空白溶液和标准品溶液的气相色谱图如图4和图5所示,EO和ECH的峰形尖锐,分离效果良好,说明该检测方法的专属性强。
图4 空白溶液的气相色谱图
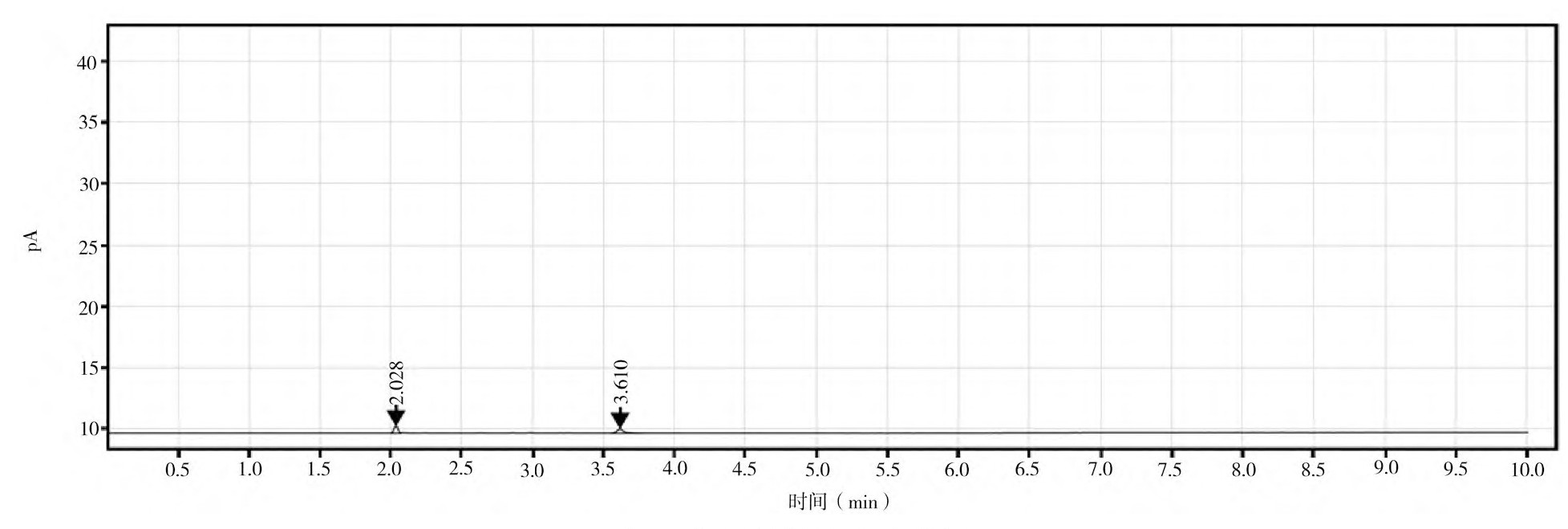
图5 EO和ECH标准品溶液的气相色谱图
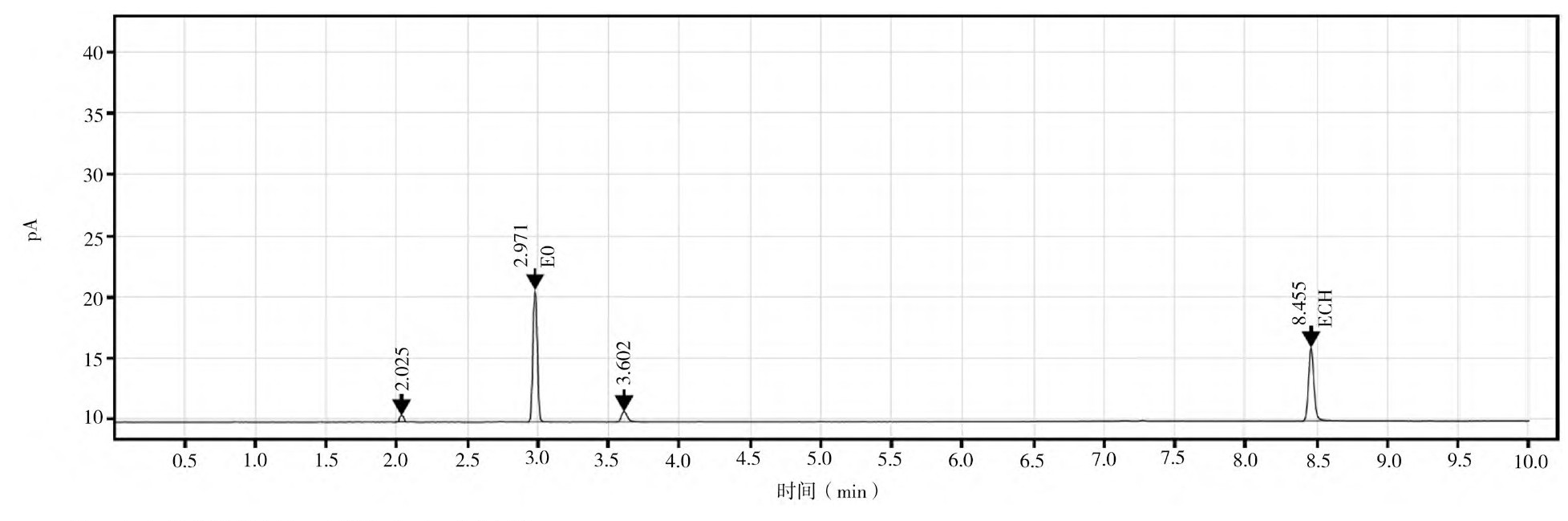
注:EO为环氧乙烷,ECH为2-氯乙醇
2.2 线性关系与检出限、定量限验证结果
以标准品溶液的浓度为横坐标,色谱峰面积为纵坐标绘制标准曲线,见图6和图7,得到EO和ECH的线性回归方程和相关系数见表1。由表1可知,EO在浓度0.25~20.00μg/ml范围内线性关系良好,ECH在浓度2.50~200.00μg/ml范围内线性关系良好
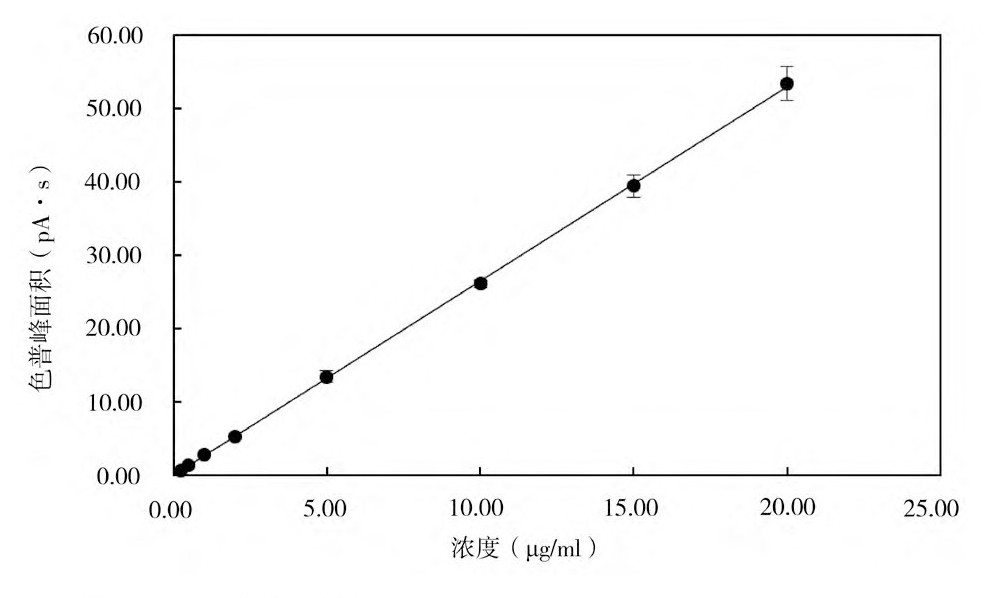
注:EO为环氧乙烷
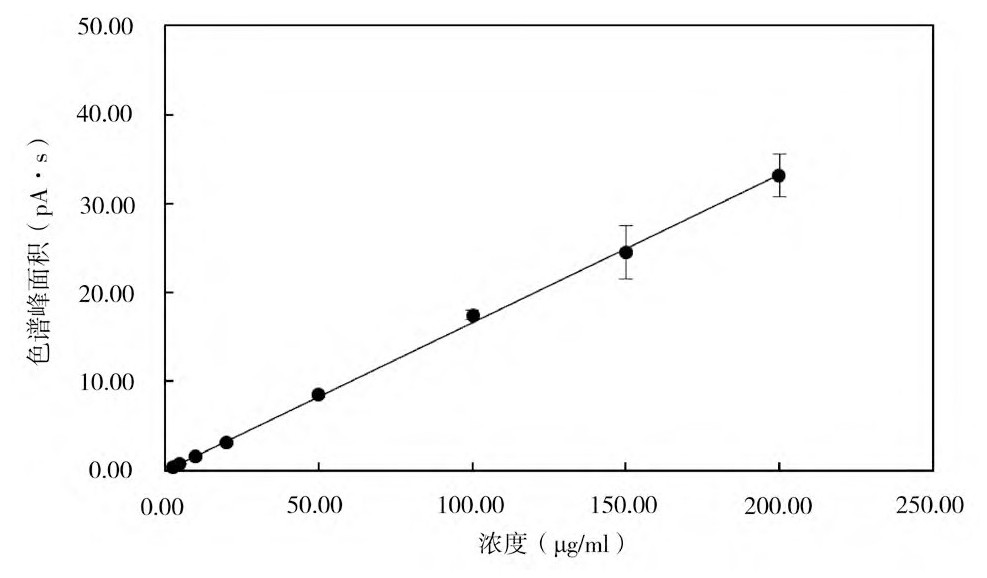
注:ECH为2-氯乙醇
表1 EO和ECH的线性回归方程和线性相关系数

注:EO为环氧乙烷,ECH为2-氯乙醇
通过逐级稀释标准品溶液重复检测,最终确定EO的检出限为0.03μg/ml,定量限为0.08μg/ml;ECH的检出限为0.50μg/ml,定量限为1.50μg/ml。
2.3 精密度验证结果
EO的精密度相对偏差为2.58%~6.78%,ECH的精密度相对偏差为2.62%~9.27%。两者的精密度均良好,满足检测要求。
2.4 回收率验证结果
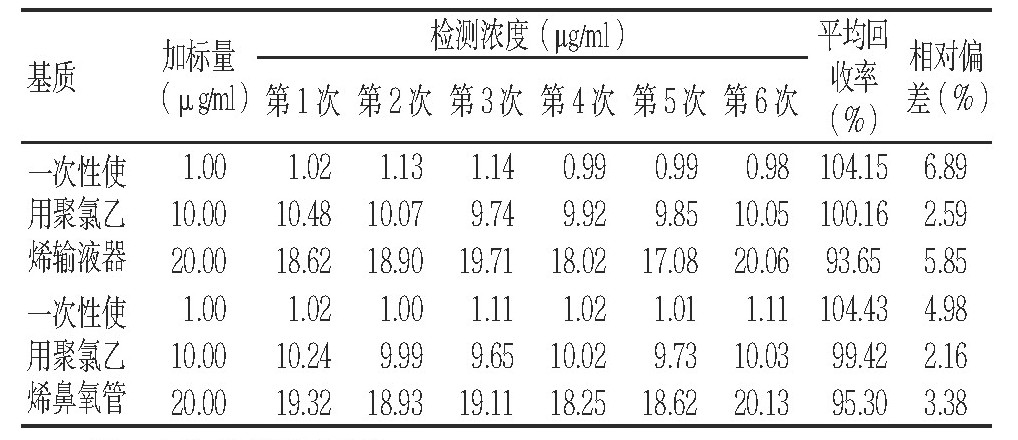
如表2和表3所示,EO在2种空白基质不同添加水平的平均回收率为93.65%~104.43%,相对偏差为2.16%~6.89%;ECH在2种空白基质不同添加水平的平均回收率为87.37%~103.83%,相对偏差为3.23%~7.22%,均满足检测要求。
表2 EO在2种基质中的回收率和相对偏差
注:EO为环氧乙烷
注:ECH为2-氯乙醇
2.5 典型产品检测结果
共2个样品检出EO,其中一次性使用聚氯乙烯输液器中EO含量为0.22μg/g,医用棉垫中EO含量为2.60μg/g;所有产品均未检出ECH。
3 结论
EO属于易挥发性有机化学物质,在灭菌领域应用广泛。1994年,国际癌症研究机构(International Agency for Research on Cancer,IARC)依据EO的作用机制将其划分为一类致癌物质[5]。GB/T14233.1-2022《医用输液、输血、注射器具检测方法第1部分:化学分析方法》[6]中明确规定了输注器具等一次性使用无菌医疗器械的EO残留量检测方法和浸提条件。ECH是EO与氯离子结合的产物,也是一种具有挥发性、类似醚臭的甘油样液体,同样对人体有害。医疗器械领域采用EO灭菌的一次性使用无菌产品种类繁多,但目前尚未形成可同时检测EO和ECH残留量的系统性方法。
顶空-气相色谱法和气相色谱-质谱联用法可同时检测EO和ECH的残留量,但目前多集中于食品和药品领域。王澍等[7]通过顶空-气相色谱法建立了食品中EO和ECH残留量的检测方法,该方法对设备的要求较低、操作简便高效,具有线性范围宽及回收率、灵敏度和准确度均较高的优势;周云婷等[8]采用顶空-气相色谱法建立了可同时检测明胶空心胶囊中EO和ECH残留量的方法,该方法前处理简单,检测灵敏度高且精密度良好;周静等[9]采用顶空-气相色谱-质谱联用技术以及离子扫描模式实现了对乳及乳制品中EO和ECH残留量的准确定性和定量检测,能够满足乳及乳制品复杂基质中EO和ECH残留量的检测要求;巩凡等[10]建立了可同时检测方便面中EO和ECH残留量的气相色谱-三重四极杆质谱法,该方法适用于食品基质,且具有较好的检测准确度和灵敏度。
由于顶空-气相色谱法是对顶空瓶中的气体部分进行分析,可有效避免样品溶液中复杂物质对色谱柱的干扰[11]。此外,气相色谱仪相较于气相色谱-质谱联用仪具有价格优势,是目前EO检测的主流仪器。因此,本研究选择顶空-气相色谱法进行EO和ECH的同时检测。但是与气相色谱-质谱联用法相比,顶空-气相色谱法需要排除目标组分和基质、溶剂的相互干扰[12]。本研究通过色谱柱的选择、气相色谱仪条件的选择,并经图4和图5的验证,排除了目标组分和基质、溶剂的相互干扰。
顶空-气相色谱法的浸提介质、平衡温度、平衡时间和浸提比例均可直接影响检测结果。经查阅文献发现,EO和ECH检测选用的浸提介质包括水[8]、丙酮[16]、乙腈[10]等,而国家标准GB/T16886.7-2015《医疗器械生物学评价第7部分:环氧乙烷灭菌残留量》[4]中明确提到通常用水作为浸提介质检测EO和ECH的残留量。因此,本研究选用水作为浸提介质。为了选择适宜的平衡温度、平衡时间及浸提比例,本研究考察了不同条件色谱峰面积的变化,最终确定了最佳平衡温度为80℃、平衡时间为30 min、浸提比例为0.5 g/ml。
本研究结果显示,所建立的顶空-气相色谱法的专属性强;EO在浓度0.25~20.00μg/ml范围内线性关系良好,ECH在浓度2.50~200.00μg/ml范围内线性关系良好;EO的检出限为0.03μg/ml、定量限为0.08μg/ml,ECH的检出限为0.50μg/ml、定量限为1.50μg/ml;EO和ECH的精密度均良好,满足检测要求;EO和ECH在2种空白基质不同添加水平的平均回收率均满足检测要求;典型产品中检测共2个样品检出EO,其中一次性使用聚氯乙烯输液器中EO含量为0.22μg/g,医用棉垫中EO含量为2.60μg/g,均低于10μg/g。所有产品均未检出ECH。此外,各类产品检出的EO残留量存在较大差异,这可能是各种材料吸收、保持和释放EO的能力存在显著差异造成的[17]。非聚氯乙烯产品未检出EO的原因可能是由于产品本身不含氯离子,在医疗器械规范生产、灭菌、存储、运输、使用等环节中,其他途径引入氯离子的可能性较低,这与非聚氯乙烯材质的经皮腔内血管成形术(percutaneous transluminal angioplasty,PTA)球囊扩张导管中ECH残留量的检测结果一致[18]。
通 过确认最佳顶空条件建立的顶空-气相色谱法可同时检测EO灭菌的一次性使用无菌医疗器械产品中EO和ECH的残留量。该方法具有操作简单、专属性强、定量准确、重现性好的特点,能够快速、灵敏检测EO和ECH的残留量,可作为一次性使用无菌医疗器械产品现行标准的有益补充。